当科では、関節リウマチや膠原病をはじめとする自己免疫疾患の診断・治療法の向上を目指し、臨床研究と基礎研究の両面から取り組んでいます。日常診療で得られる知見をもとに、病態解明や新規治療法の開発へとつなげる「トランスレーショナルリサーチ」を推進し、全国規模の多施設共同研究にも積極的に参加しています。
臨床研究
関節リウマチに関する臨床研究
未治療関節リウマチにおける炎症性メディエーターの解析
私たちの研究室では、未治療の関節リウマチ患者(RA)を対象に、免疫細胞が産生する炎症性メディエーター(サイトカインやケモカイン)が病気の進行にどのように関わるのかを明らかにする研究を行っています。RAは患者ごとに症状の現れ方や進行速度、治療への反応が異なり、その背景には免疫学的な多様性が存在すると考えられています。この多様性を整理することは、将来的な個別化医療につながる重要な課題です。
広島県内で実施された多施設共同RAレジストリー(Three Arrow Study)に登録された未治療RA患者の血液サンプルを用い、治療開始前と半年後に炎症性メディエーターの濃度を測定しました。そして治療開始から1年後に撮影したX線画像で関節破壊の進行度を評価し、両者の関連を解析しました。その結果、抗CCP抗体の有無によって、関節破壊に関わる炎症因子が異なる傾向を示すことが示唆されました。
さらに別の解析では、複数の炎症性メディエーターを組み合わせて患者をグループ分けし、それぞれに特徴的な炎症経路が関わっている可能性を見出しました。こうした結果から、RAの病態は一様ではなく、異なる経路が関節炎や関節破壊に寄与していることが示唆されます。このように、血液検査を通じてRAの炎症の多様性を捉え、病態の違いを整理することは、今後の個別化治療を実現するための基盤になると考えています。
メトトレキサート投与中の膠原病・リウマチ性疾患における葉酸補充の至適用量を検討する研究
2023年度版 関節リウマチ(RA)におけるメトトレキサート(MTX)使用と診療の手引き(日本リウマチ学会)によると、「MTXは原則、経口投与では、6-8mg/週で開始する。MTXは1週間に1回または2-3回に分割して1-2日間かけて投与する。MTXには用量依存性の副作用として主に口内炎、消化器症状、肝障害があり、これらを予防する目的で葉酸5mg/週をMTX最終投与から24-48時間後に投与する。用量依存性の副作用が出現する場合は、MTXを減量もしくは葉酸を10mg/週まで増量を検討すること。」とされています。しかし、葉酸10mg/週でMTX副作用が改善するか、MTXの効果に影響はないのか、について今まで検討されておらず根拠が十分ではありません。そのため、実臨床ではMTXの副作用が出現した際に、葉酸増量でなくMTXの減量が選択されることも多い状況です。
そこで本研究は、MTX投与中の膠原病・リウマチ性疾患の患者さんにおいて、至適な葉酸の補充量を明らかにし、異なる葉酸の補充量がMTXの副作用発生率や治療効果に与える影響を検討することを目的としました。単施設並行群間ランダム化比較試験であり、臨床研究法下の努力義務研究としてjRCTに登録されています(jRCT1061230085)。
ARM-1はフォリアミン錠5mg 2錠/週を投与する葉酸増量群、ARM-2はフォリアミン錠5mg 1錠/週を投与する葉酸標準量群です。主要評価項目は両群における治療開始12週後における肝障害の発生率の差です。副次評価項目は、ARM-1群でのベースラインと12週時点における肝酵素の変化、またMTXの代謝物である赤血球中polyglutamate化MTX(MTX-PG)濃度とRA疾患活動性、MTXによる肝障害、葉酸補充量との関連です。
本研究は、今まで明らかになっていないMTX治療下における至適な葉酸補充量を検討する点、代謝産物MTX-PG濃度と副作用の関連を明らかにする点が独創的です。葉酸10mg/週の補充がMTXによる副作用を軽減し、かつMTXの効果が減弱しないことが判明した場合、実臨床において、1.MTXの副作用が出現した際にMTXの減量より葉酸の増量を優先的に選択 2.MTX副作用リスクが高い患者では、MTX開始初期から葉酸5mg/週でなく10mg/週の併用を選択 の2点を支持するエビデンスになります。本研究の成果により、最適な葉酸の補充量の観点から、副作用が少なく効果的なMTX治療の提案が可能になることが期待されます。
関節リウマチにおける抗CCP抗体の親和性成熟と歯周病の関連に関する研究
富山大学免疫学講座を中心とした共同研究に当科も参加し、その成果が国際誌 Arthritis & Rheumatology に掲載されました。(Arthritis & Rheumatology, 72(12):2040-2049, 2020.)
この論文は、関節リウマチ患者から得られた抗シトルリン化タンパク質抗体(ACPA)の一種であるCCP-Ab1が、どのようにして病原性を獲得するのかを分子レベルで解明しています。研究では、歯周病の原因菌であるポルフィロモナス・ジンジバリス由来のシトルリン化ペプチドが、ACPAの親和性成熟を促進し、関節炎を悪化させる機能を持つことを明らかにしました。この発見は、口腔内の慢性炎症が、自己抗体の病原性を高めることで関節リウマチの病態形成に深く関与しているという、重要な免疫学的メカニズムを示唆しています。
関節リウマチにおける関節破壊とmicroRNAの関係
関節リウマチ(RA)の治療は日々進歩していますが、すべての方に同じ治療薬が効くわけではありません。特に、標準的なRA治療を受けていても関節破壊が進行してしまう患者さんも一定いることが昨今問題となっています。当科では、RAの病態への関与が注目されているmicroRNAが骨破壊の予後予測に有用かどうか、についてMIRACLE study(メトトレキサート未使用のRA患者におけるアダリムマブ追加投与時のメトトレキサート至適用量に関する多施設共同研究)のデータを用いて解析しました。
私たちは、この研究の成果が患者さん一人ひとりに最適な治療法を早期に選択する個別化医療の実現に繋がることを期待しています。
関節リウマチにおける最適な治療薬選択をめざして
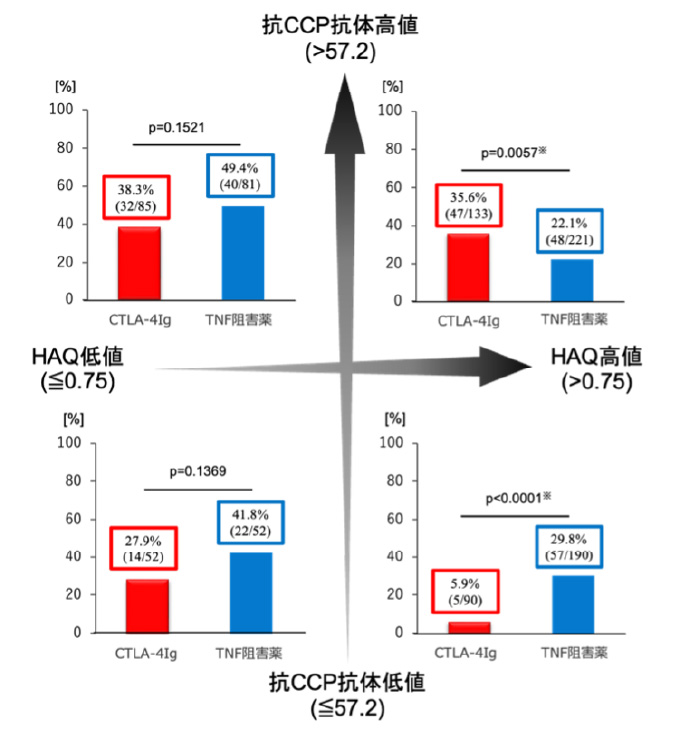
関節リウマチ(RA)は関節の炎症が続くことで関節破壊や機能障害を招く病気です。近年は生物学的製剤やJAK阻害薬など新しい薬の登場で治療成績が向上しましたが、患者さんごとに最適な薬の選択は十分に分かっていません。
私たちは産業医科大学と共同で「FIRSTレジストリ」に登録された953名の患者さんを解析し、初回治療薬としてCTLA4-Ig(アバタセプト)とTNF阻害薬を比較しました。
その結果、HAQ-DIスコアが低い患者さんでは両薬剤とも有効性に差はなく、スコアが高い場合には抗CCP抗体が高値ならCTLA4-Ig、低値ならTNF阻害薬が有効であることが分かりました。(Rheumatology, 00:1-8, 2024.)
この成果は、患者さんの背景に応じた薬剤選択、すなわち「プレシジョン・メディシン」に向けた重要な一歩です。今後は治療効果を高め、副作用や医療費負担を減らす個別化医療の実現を目指していきます。
プレスリリースはこちらからご覧いただけます
[プレスリリース(2024年12月2日)PDF] — 広島大学公式サイトより
SLEに関する臨床研究
血清補体価(CH50)低値は難治・再発性ループス腸炎の予測因子である
全身性エリテマトーデス(SLE)の稀な消化管合併症であるループス腸炎は、腹痛や嘔吐など、非特異的な症状で発症し、診断や活動性把握が難しい一方で、消化管穿孔・出血を引き起こし、生命を脅かす可能性がある病態です。
本研究は難治性・再発性ループス腸炎の予測因子を明らかにすることを目的とした後向き観察研究です。
当科で2009年から2019年の間にループス腸炎と診断された13人の患者さん(17件のループス腸炎のエピソード)が対象となりました。それぞれ治療反応良好群と治療反応不良(難治・再発)群に分け、両群の臨床的特徴、画像所見、血液検査データを比較検討しました。また、「難治」とは寛解達成のために導入療法の強化が必要な状況を、「再発」は寛解達成後のループス腸炎の増悪を示します。
主要な結果として、血清補体価が治療反応不良群で有意に低いことが明らかになりました(治療反応良好群 vs. 治療反応不良群の中央値: 29.2 [25.3–46.9] U/mL vs. 19.3 [7.8–24.0] U/mL, p=0.0095)。多変量解析でも、血清補体価が治療反応不良の独立した予測因子であることが示されました (p=0.0329)。ROC曲線解析では、血清補体価のカットオフ値28.0 U/mLが、治療反応不良を予測する上で100%の感度と77.8%の特異性を示しました。
さらに、治療反応不良群の患者さんは、中等量用量のグルココルチコイド(GC)で治療を開始された割合が有意に高く、高用量GCが良好な治療反応に関与する可能性が示唆されました (p=0.0034)。なお腹部CT所見に関しては、腸管壁肥厚の程度や他のCT所見に両群間で有意な差は認められませんでした。
本研究では、ループス腸炎において血清補体価が難治・再発性の予測因子であることが示唆されました。また、高用量GCによる初期治療を行うことが、良好な結果につながる可能性を示唆しています。(Mod Rheumatol, 31:643-648, 2021.)
全身性エリテマトーデス関連マクロファージ活性化症候群におけるカルプロテクチンとNETsの関与
マクロファージ活性化症候群(MAS)は全身性エリテマトーデス(SLE)における重篤な合併病態の一つですが、MASの早期診断や活動性評価を可能にする特異的なマーカーは確立されていません。当科では、MASを示唆するマーカーとして、好中球細胞質蛋白であるカルプロテクチンとNETosis (好中球の細胞死の一種)によって放出される好中球細胞外トラップ(NETs)に着目して臨床・基礎研究を進めています。
その他膠原病に関する臨床研究
抗MDA5抗体陽性皮膚筋炎における爪郭部毛細血管異常と筋炎特異抗体
皮膚筋炎は、筋肉や皮膚に炎症が起こる自己免疫疾患の一つです。中でも、抗MDA5抗体陽性の皮膚筋炎は、急速に進行する呼吸器の病気を合併しやすく、予後が悪いとされています。近年、強力な免疫抑制療法によって患者さんの生命予後は改善しつつありますが、治療前にどのくらいの強さの治療が必要かを見極める方法は確立されていませんでした。
そこで私たちは、全身性硬化症などの自己免疫疾患で広く用いられている、爪の生え際を観察する非侵襲的な検査「爪郭部毛細血管鏡検査(NVC)」に着目しました。この検査が、抗MDA5抗体陽性皮膚筋炎の重症度予測に役立つのではないかと考え、研究を行いました。(Rheumatology (Oxford), 61(5):2006-2015, 2022.)
研究でわかったこと
本研究では、10名の抗MDA5抗体陽性皮膚筋炎の患者さんにご協力いただき、治療前のNVC所見と、治療による変化、さらに血液中の様々な因子との関連を調べました。その結果、以下の3つの重要な事実が明らかになりました。
- NVC異常は治療によって改善する:
- 治療開始後2〜17週で、異常が見られた9例のNVC所見が正常化しました。これは、NVCが治療効果を評価する指標になりうる可能性を示唆しています。
- NVCスコアは病気の活動性と関連する:
- NVCスコアは、病気の活動性を示すとされる抗MDA5抗体価やフェリチン値と逆相関することがわかりました。つまり、NVCスコアが低い(毛細血管の異常が強い)患者さんほど、病気の活動性が高い傾向にあるということです。また、肺の機能を示すFVC(努力性肺活量)とは正の相関を示しました。
- 特定の血清バイオマーカーとNVCの関連:
- 血管関連のバイオマーカーを測定したところ、M-CSFとSCFという物質が、治療前のNVCスコアと逆相関する傾向にあり、抗MDA5抗体価とは正の相関を示しました。これらの物質も、病気の活動性や重症度を反映している可能性があります。
今後の展望
今回の研究から、抗MDA5抗体陽性皮膚筋炎において、NVC所見は治療によって変化する可能性が高く、治療を開始する前のNVC評価が非常に重要であることが示されました。NVCスコアが低い患者さん、つまり爪の毛細血管に強い異常が見られる患者さんでは、予後が不良であると予測され、より積極的な治療介入が必要であると考えられます。
この非侵襲的なNVC検査が、抗MDA5抗体陽性皮膚筋炎の患者さん一人ひとりに最適な治療を選択し、予後を改善するための有効なツールとなることが期待されます。今後さらに多くの患者さんで研究を進め、NVCの有用性を確立していきたいと考えています。

ANCA関連血管炎の発症に季節が関連する
抗好中球細胞質抗体(ANCA)関連血管炎(AAV)は、代表的な全身性壊死性血管炎です。AAVは、好酸球性多発血管炎性肉芽腫症(EGPA)、顕微鏡的多発血管炎(MPA)、多発血管炎性肉芽腫症(GPA)の3つに分類されます。好中球細胞死(NETosis)によって細胞外に放出された抗原(MPOやPR3)に対してANCAが産生されるため、AAVの発症には外的素因が関わっていると考えられています。これまでにもAAV発症の季節性を調査した研究は行われてきましたが、因果関係ははっきりしていませんでした。本研究は、それを明らかにすることを目的として計画されました。
本研究では、当院を含む日本国内24施設の後ろ向き研究(J-CANVAS)から情報が収集されました。対象は2017年1月から2019年12月までの間にAAVを発症した20歳以上の患者さんです。発症は、AAVに関連した全身症状もしくは臓器障害が初めて認識された時点と定義しました。季節は気象庁の定義に基づき、3~5月を春、6~8月を夏、9~11月を秋、12~2月を冬としました。また、患者さんの居住地の郵便番号と2020年総務省の人口密度データを紐付けし、200人/km²未満を過疎地域、それ以上を都市部と分類しました。季節性については、各季節の発症数が均等に25%ずつである場合との差をカイ二乗検定で解析しました。
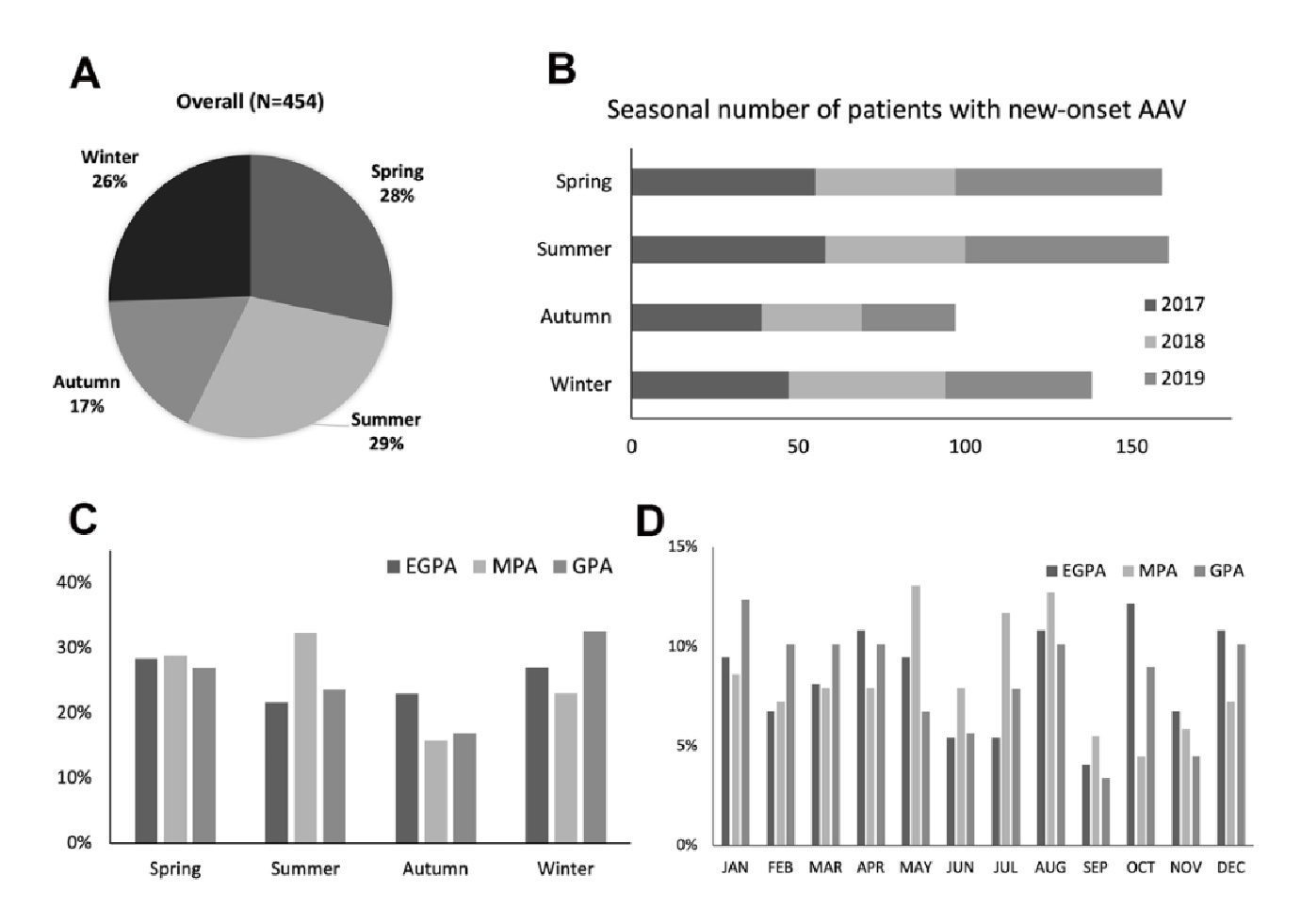
合計454例のAAV患者さん(EGPAが74例、MPAが291例、GPAが89例)が登録されました。全体の新規発症は春が28.4%、夏が28.9%、秋が17.2%、冬が25.6%であり、有意に秋の発症が少ないことが示されました(p=0.01)。この傾向は2017年から2019年までの各年でも同様でした。
ANCA別に見ると、MPO-ANCA陽性例では春が29.3%、夏が30.7%、秋が15.8%、冬が24.2%と季節性が顕著でしたが(p<0.001)、PR3-ANCA陽性例では春が21.7%、夏が26.1%、秋が26.1%、冬が26.1%と季節性を認めませんでした。
さらに、肺病変の生検が行われたAAV患者さん47例において、過疎地域の居住者の方が都市部よりも有意に肺病理での血管炎の陽性率が高かったことが分かりました(オッズ比 10.07、p=0.02)。
本研究は、AAV発症と環境素因を解析した研究として過去最大規模です。これによりAAVの発症には季節性があり、特にMPO-ANCA陽性例では秋の発症が少ないことが明らかになりました。一方、PR3-ANCA陽性例には発症の季節性がなく、血管炎による肺病変は過疎地域で認められやすいことが明らかになりました。(The Journal of Rheumatology, 50:1152-1158, 2023.)
基礎研究
試験管内合成mRNAを用いた関節炎研究への応用
当研究室では、研究時に対象となる細胞(例えば、関節リウマチの滑膜病変では滑膜線維芽細胞など)における遺伝子の機能を解析する際、遺伝子をノックダウンする場合にはsiRNAやshRNAを利用しています。また、遺伝子の過剰発現を行う場合には、プラスミドDNAの導入に加えて試験管内で合成されたmRNAを細胞に導入する方法を用いています。当研究室では、合成mRNAを用いることにより、細胞毒性が低くかつ初代培養細胞などの従来遺伝子の導入が困難であった細胞での導入も可能となりました。またこの技術はin vivoモデルでの応用も可能であり、マウスの関節腔内に合成mRNAを投与することで関節内組織に遺伝子を導入することも可能となりました。当科の研究グループでは2014年から合成mRNAについての研究を続けており、滑膜線維芽細胞での有用性について修飾核酸であるN1-メチルシュードウリジン(m1ψ)を含んだ合成mRNAの中の有用性を検討し、m1ψ含有mRNAは非含有mRNAに比べて外来発現の発現を増強しつ、同時に導入によって生じる非特異的な免疫反応を抑制することを2022年に報告しています。(Cytotechnology, 74:503-514, 2022.)
滑膜細胞における血液凝固第XIII因子の機能
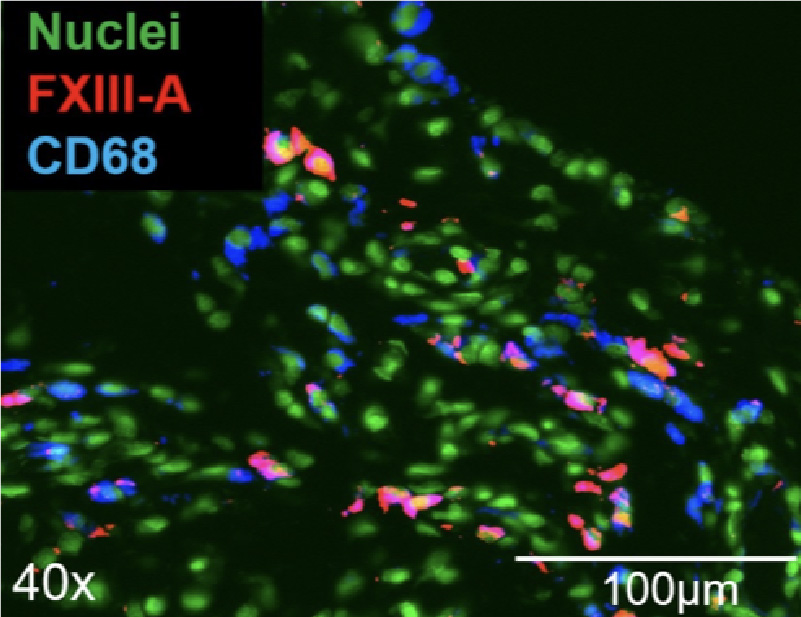 <図1>滑膜組織の免疫染色。FXIII-Aとマクロファージ
<図1>滑膜組織の免疫染色。FXIII-AとマクロファージマーカーのCD68は同じ細胞で発現している。
FXIII(血液凝固第XIII因子)は、凝固カスケードの最終段階でフィブリン同士を架橋し、血栓を安定化させる因子です。私たちは今回、滑膜組織におけるFXIIIの発現とその調節機構、特にFXIIIのBサブユニット(FXIII-B)の機能に注目しました。(Inflamm Regen, 43(1):2, 2023.)
免疫染色の結果、FXIII-AはM2マクロファージに、FXIII-Bは線維芽細胞様滑膜細胞に発現していることが分かりました(図1)。また、IL-4刺激で誘導されたマクロファージにIL-6を加えるとFXIII-Aの発現が増加し、逆に抗IL-6受容体抗体により抑制されることが明らかになりました。
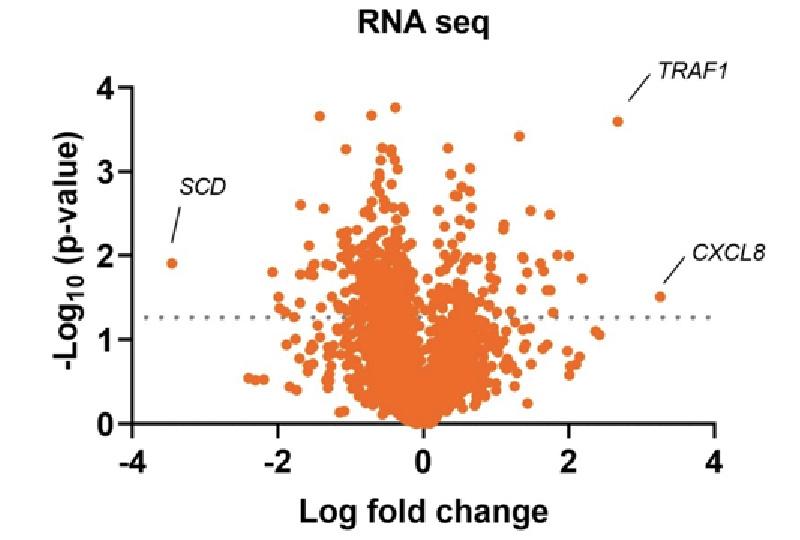 <図2>滑膜組織のRNAシーケンスデータ。FXIII-Bを過剰
<図2>滑膜組織のRNAシーケンスデータ。FXIII-Bを過剰発現した滑膜細胞ではケモカイン関連遺伝子(CXCL8)や
抗アポトーシス関連(TRAF1)の発現が亢進している。
FXIII-Bの機能を解析するために、RNAシーケンス解析を行ったところ、FXIII-Bを過剰発現させた細胞では抗アポトーシス関連分子やケモカインの発現が上昇することが分かりました(図2)。これらの結果から、滑膜がFXIIIの供給源であること、またFXIII-Aの発現がIL-6依存的に制御されていること、さらにFXIII-Bが滑膜環境で新たな機能を担っている可能性が示唆されました。現在、RAにおけるFXIIIの役割についてさらに解析を進めています。
炎症性サイトカインによって誘導されたニューロピリン2は新型コロナウイルスの増殖を促進する
COVID-19は、SARS-CoV-2というウイルスによって引き起こされる感染症であり、高齢者などのリスクの高い人々では、現在も重症化や死亡のリスクが高いことが知られています。ウイルスは主に口や鼻、消化管などから体内に入り、血流によって肺、脳、血管など多くの臓器に広がり、さまざまな障害を引き起こします。近年、ウイルスが人の細胞へ感染するためには、細胞表面の特定の受容体タンパク質(ACE2やNRPファミリー)との結合が重要であることが明らかとなっています。
当科ではウイルス変異による治療薬やワクチンの効果低下という課題に対し、ウイルス抗原に依存しない新たな治療標的の探索を目的とし、SARS-CoV-2の感染に関わる受容体NRP(Neuropilin)と、炎症性サイトカインとの関係性に注目しました。
その結果、炎症性サイトカインであるTNFαやIL-1βを培養細胞に添加すると、ヒト滑膜線維芽細胞や肺線維芽細胞において、NRP2という受容体の発現量が増加することを確認しました。さらに、NRP2は転写因子NF-κBによって調節されていることを明らかにしました。実験では、炎症性サイトカインの存在下でSARS-CoV-2に感染させた場合、NRP2の発現が増え、ウイルスの増殖も促進されることが分かりました。
加えて、NRP2を過剰に発現させた細胞ではウイルスの増殖がより顕著になり、逆にNRP2の発現を抑えることでウイルスの増殖を抑制できることも確認しました。(Viruses, 15(7):1498, 2023.)
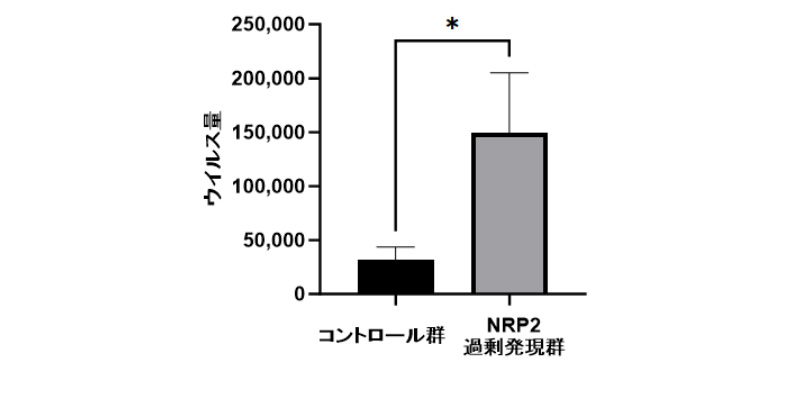 ヒト滑膜線維芽細胞においてNRP2タンパクを多量に
ヒト滑膜線維芽細胞においてNRP2タンパクを多量に発現させると、コントロール群と比較してウイルス
(SARS-CoV2)の増殖が促進されました。
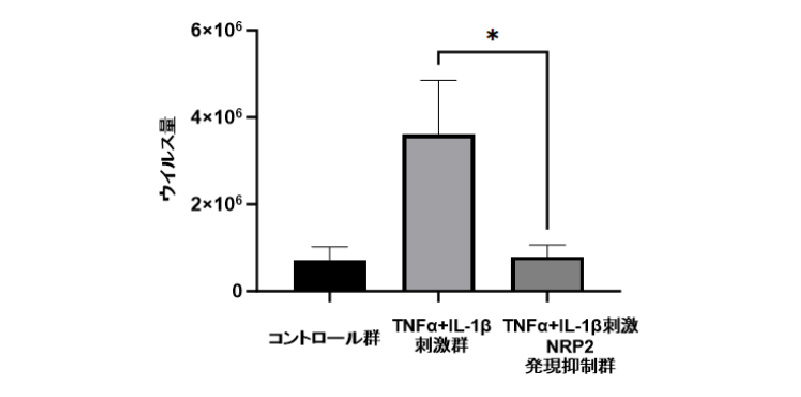 ヒト滑膜線維芽細胞においてTNFαとIL-1βの共刺激を
ヒト滑膜線維芽細胞においてTNFαとIL-1βの共刺激を行うと、コントロール群と比較してウイルス
(SARS-CoV-2)の増殖が促進されました。一方、NRP2
タンパクの発言を抑制すると、TNFαとIL-1βの共刺激を
加えてもウイルスの増殖は促進されませんでした。
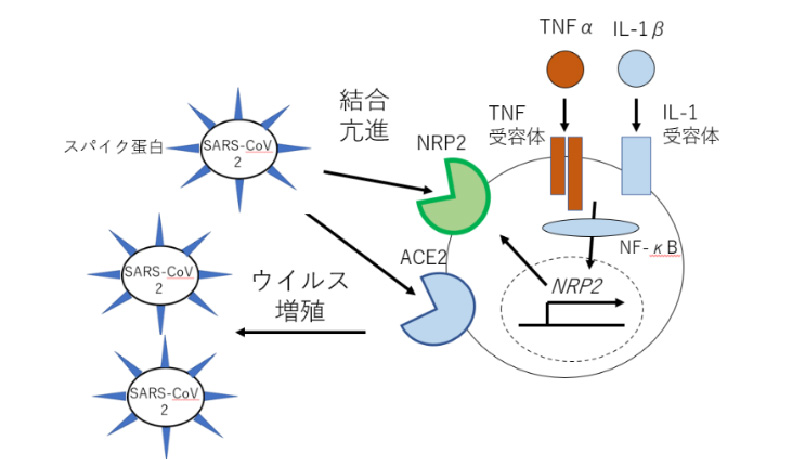
TNFα、IL-1βが細胞の周囲に高濃度に存在することにより、
ヒト線維芽細胞では転写因子NFk-Bを介してNRP2の発言が増加します。
NRP2の発言が増加すると、SARS-CoV-2とACE2の結合がNRP2によって
補助され、ウイルスが細胞内へ侵入しやすくなります。その結果ウイルス
の増殖が促進されます。
